Kapcsolódó bejegyzés
Hogyan lehet eredményeket validálni: ChIP-Seq adatelemzési folyamatának magyarázata
2026-02-27A ChIP-Seq adatelemzési csővezeték validálása az a lépés, amely a csúcsokat bizonyítékká változtatja, nem csupán képek. A Longlight Technology-nál támogatjuk a ChIP-seq projekteket mintától jelentésig, és egy egyértelmű szabályt látunk: ha megfelelő sorrendben validál, a következtetések stabilak, megmagyarázhatók és könnyebben publikálhatók lesznek.
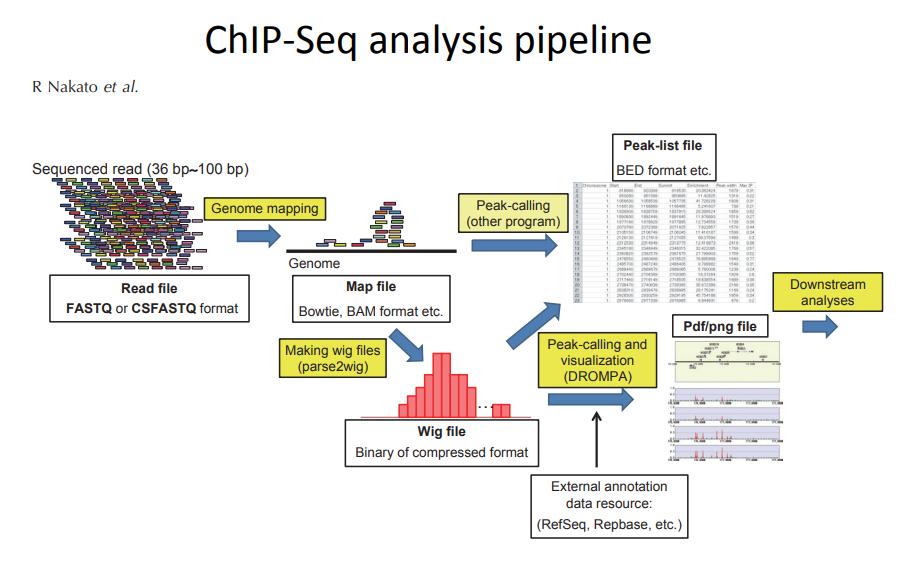
A Beginner's Guide to ChIP-Seq Data Analysis | by sezer islambey | Medium
1) Értsd meg, mit bizonyít a ChIP-Seq, egyés mit nem.
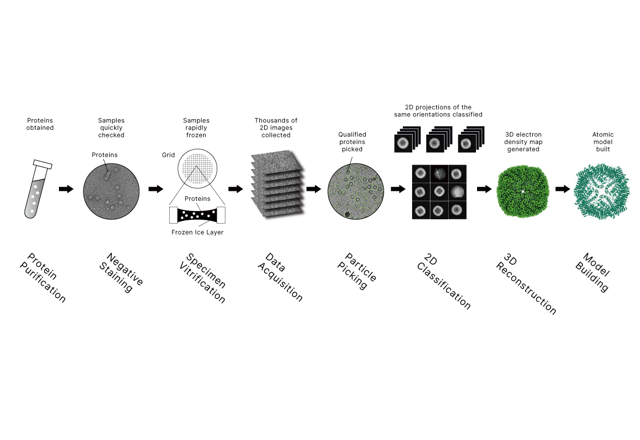
ChIP-seq egy egyszerű tudományos céllal kezdődik: mérjük, hogyan lépnek kölcsönhatásba a fehérjék a DNS-rel valós biológiai mintákban. A gyakorlatban segít feltérképezni, hol gazdagodnak a transzkripciós faktorok, RNS-polimeráz II vagy hiszton módosítások a genom területén. Egy jól kiépített ChIP-Seq adatelemző folyamatvonal olyan kérdéseket is támogathat, mint például a fehérjék jelenléte különböző genomiális helyeken, transzkripciós faktor kötődési viselkedése, valamint a hiszton jegyek viszonya a génexpresszióhoz.
A validáció fontos, mert a ChIP-seq egy összekapcsolt lépéslánc. Ha bármelyik kapcsolat gyenge – antitest-specifikusság, kromatin minőség, könyvtár komplexitása vagy háttérkontroll –, a végső csúcsok meggyőzőek lehetnek, de mégis megbízhatatlanok lehetnek. Egy kezdőbarát módja az elismerésnek a megerősítésnek: nem próbálsz "csúcsokat elérni". Azt próbálod bemutatni, hogy a csúcsok ugyanazok között a körülmények között újra megjelennének, és hogy megfelelnek a várt biológiának.
✓ A ChIP-seq a dúsítást méri, nem az abszolút kötési számokat
✓ A jó eredményekhez kontroll és ismételhetőség szükséges, nem csak a mélység szekvenálása
✓ Az ellenőrzést a kísérlet kezdete előtt kell megtervezni, nem a csúcsok meghívása után
2) Építsd be a validációt tMunkafolyamatok tAz első minta
Sok csapat csak a bioinformatika szakaszában koncentrál az érvényesítésre. Ez gyakran túl késő. A leghatékonyabb validációs megközelítés, ha már a kezdetektől részessé teszik a szolgáltatási folyamatot, mert a korai vezérlés megakadályozza a késői átdolgozást.
Kiszervezd az egész csővezetéket: fix sejtes vagy fagyasztott szövetmintákat biztosítasz; A Longlight Technology előkészítést, kromatin feldolgozást, könyvtárépítést, szekvenálást és elemzést biztosít. Az előny nem csupán a kényelem. Csökkenti az átadás kockázatát, és következetes a minőségellenőrzéseket a lépések között, így a végső ChIP-Seq adatelemzési csővezeték kimenete könnyebben megbízható.
Amikor a mintabemenet korlátozott, a validáció még fontosabb. Optimalizált folyamatunk alkalmas kis mintaméretekhez, ami segíti a kutatókat abban, hogy előrehaladjanak, amikor az anyag értékes. A gyakorlati érték az ügyfelek számára egyszerű: kevesebb mintahulladék, kevesebb próbálkozás-hiba ismétlés, és tisztább döntések a projekt elején.
✓ Egy folyamattulajdonos csökkenti a lépések közötti eltérést
✓ A szabványos ellenőrzőpontok megakadályozzák a "láthatatlan hibákat"
✓ A kis mintás készenlétszám védi a ritka szöveteket és az alacsony hozamú projekteket
3) Ellenőrizd az adatminőséget, mielőtt bármilyen csúcsban megbíznál
Egy erős ChIP-Seq adatelemzési folyamatvonal minőségellenőrzéssel kezdődik, amely egy kérdésre válaszol: képes-e az adathalmazod valódi jelet előállítani a háttér felett?
Kezdjük azzal, hogy átnézzük a gépen kívüli adatminőséget és az alapvető könyvtári viselkedést. Ha a bemeneti DNS vagy a ChIP könyvtár rendellenes olvasási minőséget, erős adapter jelenlétet vagy extrém duplikációt mutat, a csúcshívás erősítheti a zajt. A jó megerősítés nem a tökéletesség után kutat. A minták közötti konzisztenciát és a ChIP és a vezérlés közötti egyértelmű elkülönítést keresi.
Ezután ellenőrizd az igazítási viselkedést és a szűrési szabályokat. A leképezési sebesség és a használható olvasások aránya nem szabad nagyon ingadozzon a replikációk között. Ha az egyik replikált másként viselkedik, ne hagyd figyelmen kívül. Tekintsd úgy, mint egy jelet, hogy valami megváltozott a kísérletben vagy a mintakezelésben.
Kezdőknek a leggyakorlatiasabb szokás az összehasonlítás. Hasonlítsd össze:
• ChIP vs bemenet
• Replikáld A vs Replikáld B
• Kezelés vs Kontroll ugyanazok a feldolgozási szabályok szerint
Itt válik valódi értékké a "szigorú minőségellenőrzés minden linkben". Ha a minőségellenőrzést minden alkalommal ugyanúgy alkalmazzuk, gyorsan azonosíthatjuk az igazi kivételt, és elkerülheted a következtetéseket egy instabil mintára.
✓ Validáld az adathalmazt a csúcshívás előtt időt takarít meg később
✓ A következetes szűrés megakadályozza a mesterséges különbségeket
✓ A kivételeket dokumentálni kell, nem elrejteni
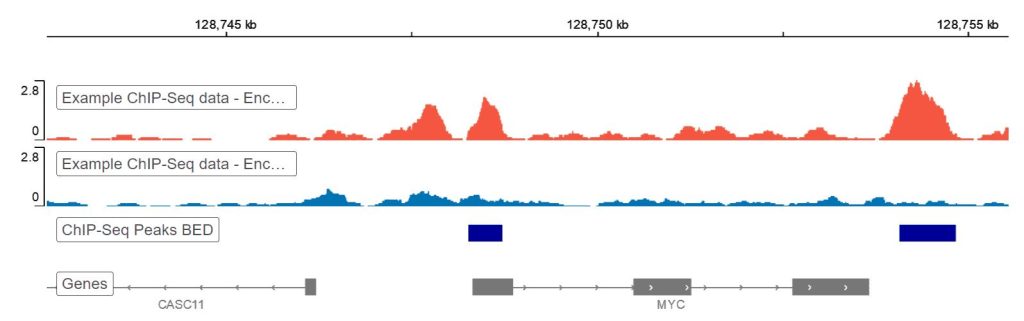
ChIP-Seq Analysis Tutorial - Basepair
4) Validáld a csúcsokat vezérlőkkel egynd célszerű logika
A csúcshívás nem egyetlen gomb. Ez egy döntési rendszer. A ChIP-seq célpont lehet keskeny kötődő transzkripciós tényező vagy szélesebb körű hisztoszmódosítás, és az validációs módszernek meg kell felelnie a biológianak.
A vezérlők az első bizonyítási réteg. A bemeneti DNS segít modellezni a háttérjeleket, és csökkenti a hamis dúsítást a nyílt kromatinból, ismétlődő régiókból vagy szekvenálási torzításból. Ha a csúcskészletek drámaian változnak, amikor a vezérlést alkalmazzák, akkor háttéralapú csúcsokat láthatsz, nem pedig valódi kötést.
Ezután validáld a csúcsforma és a dúsítási logikát. A transzkripciós faktor csúcsai gyakran élesek és lokalizáltak, míg néhány hisztonjel szélesebb régiókat képez. A várható jelforma és a megfigyelt pályák közötti eltérés ok arra, hogy újra ellenőrizzük az upstream kísérleti feltételeket, nem csak a szoftveres küszöbértékek módosítását.
A Longlight támogatja az ügyfél kutatási célja alapján meghatározott gének vagy régiók elemzését is. Sok projektnél ez a leginkább megvalósíthatóbb validációs lépés. Ha a hipotézis egy meghatározott útvonalra vagy célgenomikai régióra fókuszál, az validációnak célzott áttekintést kell tartalmaznia ezeknek a lokuszoknak, nem csak a globális csúcsszámnak.
✓ Használd az input funkciót a gazdagítás elválasztásához a háttértől
✓ Párosítás csúcsstratégiája a TF vs hiszton viselkedéshez
✓ Validáld azokat a kulcsfontosságú géneket vagy régiókat, amelyek fontosak a kutatási kérdésed szempontjából
5) A megismételhetőség igazolása bármilyen differenciális igény előtt
A legmeggyőzőbb igazolás a reprodukálhatóság. Ha a replikációk nem egyeznek meg, a "differenciális csúcsok" inkább zajról szólhatnak, mint biológiáról.
Egy gyakorlati ChIP-Seq adatelemzési csővezetéknek két szinten kell ellenőriznie a replikációs egyeztetést: a genom-szintű jelhasonlóságot és a csúcsátfedési stabilitást. Azt is megvizsgálhatod, hogy a legmagasabb rangú csúcsok továbbra is a legjobban rangsoroltak-e a replikációk között. Ha csak egy ismétlés vezérli az eredményt, a következtetésed törékeny lesz.
Kezdőknek érdemes egy egyszerű mércét felállítani: el kell tudnod magyarázni, miért számítanak megbízhatónak egy csúcs. Ez a magyarázat általában tartalmazza a replikátumok közötti állandó jelenlétet, erősebb dúsítást, mint a kontrollt, valamint a célpont típusához illő jelprofilt.
Itt a szigorú minőségellenőrzés közvetlenül segíti az ügyfeleket. Az erős minőségellenőrzés csökkenti az ismételt kísérleteket, és növeli annak az esélyét, hogy a végső jelentésed publikálható következtetést támaszt alá, nem pedig csak belső megfigyelést.
✓ A megállapodás megmásolása feltétel, nem bónusz
✓ A differenciálalízist stabil csúcsokra kell építeni
✓ "Megmagyarázható csúcsok" biztonságosabbak, mint "több csúcs"
6) A validáció átalakítása egy Jelentés, amit használhatsz egynd megosztás
Az elismerés csak akkor értékes, ha világos jelentés lesz, amelyben mások is megbízhatnak. A teljes kimenetnek tartalmaznia kell a nyers adatadást, szabványosított minőségellenőrzési összefoglalókat, csúcshívási beállításokat és a reprodukálhatóságot igazoló logikát. Az eredményeket biológiai értelmezésre is át kell ültetnie: csúcsannotáció, célterületi áttekintés és értelmes példák, amelyek kapcsolódnak a hipotézisedhez.
A Longlight Technology integrált megoldásokkal támogatja a modern genomikát – NGS-hez kapcsolódó eszközökkel, reagensanyagokkal és laboratóriumi munkafolyamatokkal, amelyeket akadémiai, klinikai és ipari környezetben használnak. A gyakorlatban ez azt jelenti, hogy a kutatók a kísérleti végrehajtást a lefelé irányuló elemzési szabványokhoz igazíthatják, ahelyett, hogy különálló világként kezelnék őket. Emellett széles körben használt fogyókat és készleteket is biztosítunk, mint például Qubit-csövek, nukleinsav-kivonási készletek és könyvtárelőkészítő készletek, amelyek stabil munkafolyamatokat támogatnak több projekttípus között.
CTA (Call-To-Action): Ha olyan ChIP-seq projektet szeretnél, amelyet lépésről lépésre validálnak – a mintakezeléstől a teljes adatjelentésig –, vegye fel a kapcsolatot a Longlight Technology-vel, hogy kérjen műszaki konzultációt és ingyenes árajánlatot. Célosan kidolgozott validációs ellenőrzőlistát biztosítunk a célkategóriád számára, és biztosítjuk, hogy a kontrollok és a jelentések egyeztek meg a szekvenálás előtt, hogy zökkenőmentes a lefelé vezető munkafolyamat.
• Kérjen egy integrált ChIP-seq tervet, amely összhangban van kutatási céljaidhoz
• Prioritási gének/régiók jelölése célzott elemzéshez
• Teljes jelentések nyers adatokkal és validációs összefoglalókat szerezzen