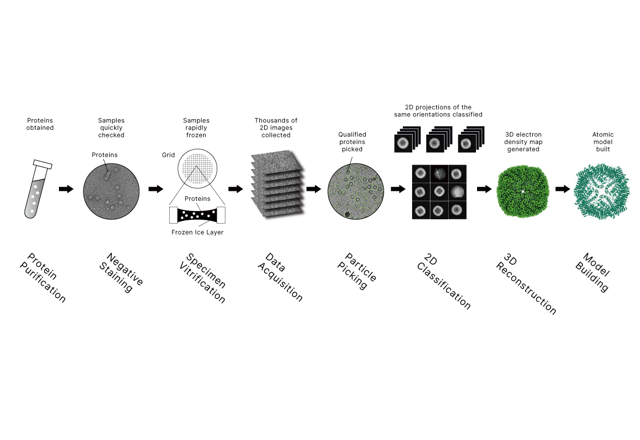
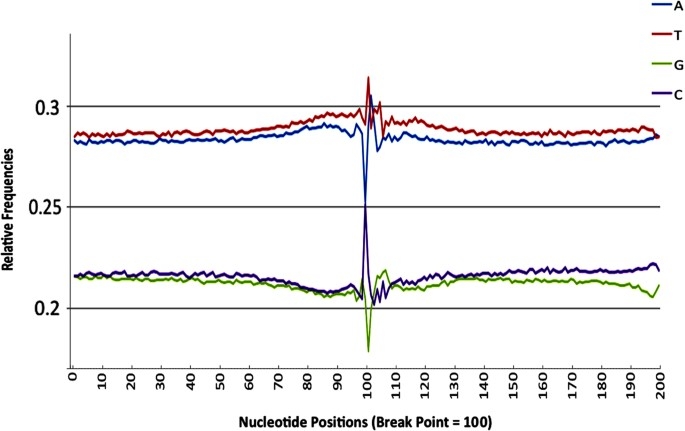
Kapcsolódó bejegyzés
Mit tanít a MS keresztkötése fehérjekomplexek számára a konformációs változásról
2026-02-22Cross-Linking MS for Protein Complexes is one of the most practical ways to "freeze" real protein contacts in place and then read them out by mass spectrometry—so you can learn how a complex changes shape, not just what it looks like in one snapshot. At Longlight Technology, we see many teams start with a simple question: Is my protein complex static, or is it switching between conformations that matter for function? This article explains, in a beginner-friendly way, what chemical cross-linking coupled with mass spectrometry (often called CL-MS or XL-MS) can teach you about conformational change, and how to turn results into decisions you can act on.
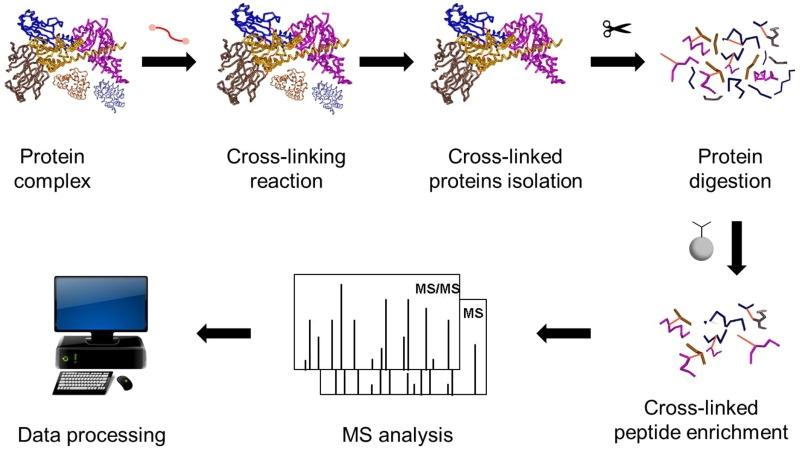
Fejlődés a fehérjekomplex elemzésben kémiai keresztkötéssel és tömegspektrometriával
1) Mi az a keresztlinkelési MS?
Keresztkötelék MS (gyakran XL-MS vagy CL-MS formátumban írva) is a method that helps you find which parts of proteins are close to each other—either within one protein or between proteins in a complex—by chemically "linking" them and then identifying those links by mass spectrometry.
Íme az ötlet egyszerű angolul:
• Add a cross-linker (a small chemical "bridge")
Specifikus aminosavakkal reagál, és kovalentálisan képes összekapcsolni két egymástól korlátozott távolságban lévő maradványt.
• A fehérjék peptidekké történő emésztése
Az enzimek (gyakran trippin) kisebb darabokra vágják a fehérjéket.
• Tömegspektrometria futtatása
Az MS peptideket érzékel, beleértve a keresztkötődő peptid párokat is.
• Elemezze a keresztkapcsolatokat
Minden azonosított keresztkötés távolsági korlátvá válik:
"Residue A and residue B were close enough to be linked under these conditions."
Mire használják
• Fehérje–fehérje kölcsönhatás (PPI) leképezése: ki érinti kit egy komplexumban
• Interfész azonosítás: mely területek alkotják a kontaktfelületet
• Konformációs változás: összehasonlítsa a feltételeket (apo vs ligandhoz kötött, mutáns vs WT), hogy lássuk a kontaktusok megjelenését vagy eltűnését
• Támogató szerkezeti modellezés: kombinálva krio-EM/X-ray modellek validálására vagy finomítására
Miért értékes
• Can capture weak or short-lived interactions (the covalent link "freezes" them)
• Gyakran nem szükséges külön címkézés
• Viszonylag nagy áteresztőképességű lehet több feltétel összehasonlításához
2) Miért olyan nehéz a konformációs változás To Elfogás
Sok fehérjekomplexum nem áll mozdulatlanul. Légznek, fordulnak, nyitnak, zárnak és újrarendeznek alegységeket a ligandokra, sóra, pH-ra, foszforilezésre vagy kötőpartnerekre reagálva. A hagyományos szerkezeti módszerek kiválóak lehetnek, de gyakran a stabil állapotokat részesítik előnyben. Ha egy komplexum rugalmas, gyengén összerakott vagy rövid életű, akkor csak a történet egy részét láthatod.
Cross-linking helps because it can covalently connect two residues that come within a certain distance. In plain language, it marks "these two positions were close enough to touch" at the time of reaction. Side-by-side cross-link comparisons—ligand-free vs bound, low vs high salt, wild-type vs mutant—tell you if the complex compacts, expands, or reconfigures.
✅ Gyakorlati betekintés kezdőknek: a konformációs váltások együttes váltások. Az XL-MS a legstabilabb konformáción túlmutat a oldatban lévő állapotok spektrumán.
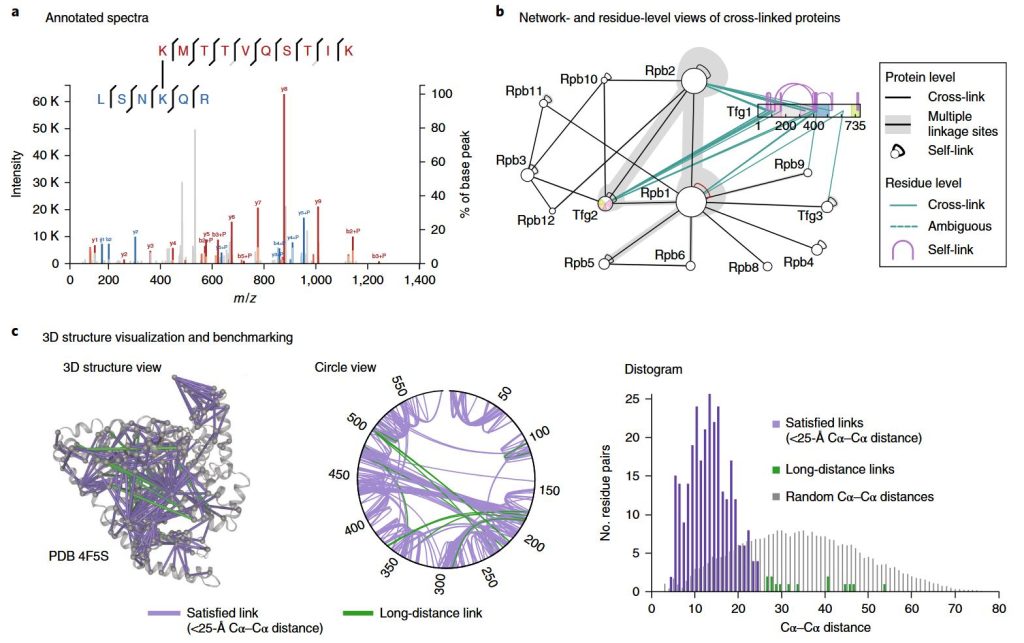
Keresztkötési tömegspektrometria szolgáltatás | MtoZ Biolabs
Milyen keresztkötési MS mérések a gyakorlatban
A kémiai keresztkötés MS-szel kvantifikálja a maradék közelségét és kölcsönhatási mintázatait, ami egy szabványos megközelítés a PPI-k tanulmányozásában. A keresztkötő anyagok reagálnak a fehérjék funkcionális csoportjaival, és összeköthetnek két vagy több kölcsönhatásos fehérjét (vagy két pozíciót egy fehérjén belül). A keresztkötés után a tömegspektrometria elemezi a keresztkötő peptideket, lehetővé téve az interakcióhálózatok ábrázolását és az akcióhelyek azonosítását.
Mit jelent ez a konformációs változás szempontjából?
• Ha egy keresztkötési halmaz csak ligandkötés után jelenik meg, az új érintkezések keletkezését jelzi a kötött állapotban.
• Ha bizonyos keresztkapcsolatok eltűnnek, az arra utal, hogy ezek az oldalak már nem közel állnak egymáshoz – talán a komplexum megnyílik, vagy egy domain elköltözik.
• Ha a keresztkapcsolatok az alegységek között elmozdulnak, az alegységek átrendeződését vagy más összeszerelési útvonalat jelezhet.
✅ Mit nyersz ebből a módszerből (és miért számít ez):
• Nem szükséges külön vegyi címkézés, → a fehérjét közel tarthatja eredeti formájában, és csökkentheti a kísérleti költségeket.
• Rövid életű/gyenge kölcsönhatásokat rögzít, → kovalens kötések megőrizhetik azokat a kontaktusokat, amelyek egyébként szétesnek a tisztítás vagy elemzés során.
• Nagy áteresztőképesség és gyors elemzési sebesség → hasznos, amikor sok feltételt vagy konstrukciót kell hatékonyan összehasonlítani.
• Sejten belüli keresztkötés lehetséges, → egyes projektek esetében ez segít a komplexumok tanulmányozásában, amely közelebb áll a saját sejtkontextusukhoz, nem csak in vitro környezetben.
4) Olvasás "Mozdulat" Keresztkötési mintákból
A kezdők néha azt várják, hogy egy keresztkötés egyenlő egy válasz. A gyakorlatban az érték a mintákból fakad.
Egy hasznos gondolkodásmód: a keresztkapcsolatok távolsági korlátok. Amikor egy komplex konformációja megváltozik, a két maradék közötti távolság is változik. Az XL-MS nem mindig tudja pontosan megmondani a forgásszöget, de meg tudja mondani, hogy a régiók valószínűleg közelebb vagy távolabb helyezkedtek egymástól, és hogy az interakciós leképezés megváltozott-e.
Íme a gyakori konformációs történetek, amelyeket az XL-MS feltárhat:
✅ Tömörítés vs nyitás
Ha több fehérjén belüli keresztkapcsolatokat látunk távoli régiókban egy feltétel alatt, a fehérje talán kompaktabb állapotot vesz fel. Ha ezek a linkek eltűnnek, míg mások emelkednek, akkor lehet, hogy megnyílik.
✅ Interfész kapcsoló
Ha az A és B alegység keresztkapcsolatai gyengülnek, míg az A és C közötti kapcsolatok erősödnek, az átsúlyozott összeszerelést vagy interfészkapcsolót javasol.
✅ Stabilizáció liganddal vagy mutációval
A ligand that "locks" a conformation often increases the reproducibility of a specific cross-link set and reduces mixed patterns.
Gyakorlati szempontból ez irányíthatja a következő lépéseket: melyik mutánst kell létrehozni, melyik tartományt vágjuk le, melyik pufferállapot stabilizálja a komplexust, vagy melyik interfészt érdemes más módszerrel validálni.
5) Erősebb eredmények, ha az XL-MS-t krio-EM vagy röntgenrel kombináljuk
Az XL-MS-t gyakran használják krioelektronmikroszkópiával (cryo-EM) és röntgenkristálydiffrakcióval együtt biológiai szerkezeti kutatásokban. Ez a kombináció különösen hasznos, ha a konformációs változás a fő kérdés.
• A krio-EM strukturális modellt nyújthat a domináns állapotok számára.
• Az XL-MS igazolhatja, hogy egy modell összhangban van-e a megoldás viselkedésével, és jelölheti meg alternatív állapotokat, amelyeket a krio-EM alulmintázhat.
• X-ray képes nagy felbontású domaineket szolgáltatni, míg az XL-MS segít a domaineket rugalmas összeállításban elhelyezni.
✅ Egy gyakorlati munkafolyamat: először használd az XL-MS-t, hogy megtudd, a komplexed heterogén-e. Ha igen, akkor olyan feltételeket tervezhetsz, amelyek gazdagítanak egy államot, mielőtt nagy felbontású szerkezeti munkába fektetnél.
6) A szolgáltatási munkafolyamat Egyt Longlight Technology
Sok labor szeretné megtudni a Cross-Linking MS for Protein Complexes alkalmazásáról anélkül, hogy teljes vezetéket építene ki saját házon belül. A Longlight Technology támogatja a tapasztalt csapatokat és az első felhasználókat is világos szolgáltatási folyamattal.
Küldhetsz kereszthivatkozási mintákat, vagy felveheted velünk a kapcsolatot, hogy keresztkapcsolati tervet dolgozzon ki, majd mintákat küldj. Teljes munkafolyamatot elvégezünk, beleértve az enzimemésztetést, peptidgazdagítást, tömegspektrometria detektálását, adatelemzést és kísérleti jelentés benyújtását. Ez a végponttól végpontig megközelítés fontos, mert a konformációs értelmezés a lépések közötti következetes kezelésen alapul.
✅ Mit jelent ez Önnek, mint ügyfélnek:
• Fewer handoff errors between steps, and fewer "unknowns" when you compare conditions
• Egy olyan jelentés, amely gyakorlati értelmezésre épül, nem csak nyers azonosításokra
• Gyorsabb iteráció, amikor több konstrukciót vagy kezelési feltételt kell tesztelni
Ha a tágabb projekted genomika vagy upstream próbafejlesztést foglal magában, a Longlight korszerű genomikai megoldásokat, fejlett laboratóriumi eszközöket, valamint magas minőségű reagenseket és fogyókat is kínál, amelyek a modern laborok hatékonyságának és pontosságának javítására szolgálnak – támogatva a kutatási munkafolyamatokat a molekuláris biológiától a precíziós elemzésig.
7) Gyakorlati CTA: Alakítsuk a konformációs kérdéseket tesztelhető bizonyítékká
A konformációs változás nem mellékrészlet. Gyakran eldönti, hogy a célpont gyógyszerezhető-e, hogy egy komplex megfelelően áll-e össze, és valóban zavaró-e a mutáció. A Cross-Linking MS for Protein Complexes bizonyítékot ad arra, hogy összehasonlítható feltételek között, ami segít abbahagyni a találgatást és elkezdeni a tervezést.
✅ If you are planning a conformational-change study, consider starting with one "comparison set":
• Apo vs ligandhoz kötött (vagy inhibitorhoz kötött)
• Vadtípus vs egy interfész mutáns
• Egy stabilizáló puffer vs egy feszültségnövelő puffer (só/pH tartomány)
CTA: Ha világos, kezdőbarát XL-MS tervet szeretnél, amely a fehérjekomplexodhoz szabott, vedd fel a kapcsolatot a Longlight Technology-vel, hogy megbeszéld a célodat (interakciós térképezés, interfész validálás vagy konformációs összehasonlítás). Segíthetünk Önnek egy gyakorlati keresztkapcsolati stratégia kiválasztásában, és egy értelmezhető jelentést nyújthatunk, amely támogatja a következő kísérletét – vagy a következő szerkezeti modelljét.