Kapcsolódó bejegyzés
Miért gyorsítja fel az XL-MS a gyógyszercél felfedezését
2025-12-25The Drug Target Discovery is the process of finding the specific molecules in the body that a new medicine should act on. Successful cancer therapies, many kinase inhibitors, and immune checkpoint drugs like PD-1/PD-L1 antibodies all began with Drug Target Discovery breakthroughs. Researchers look for proteins that drive disease, validate their role, and then design small molecules or biologics to modulate them. Yet as diseases become more complex, traditional methods often struggle to reveal the right targets at the right time. How can we see protein interactions more clearly, in real biological environments, and move from candidate to confirmed target faster? This is where XL-MS begins to change the game...
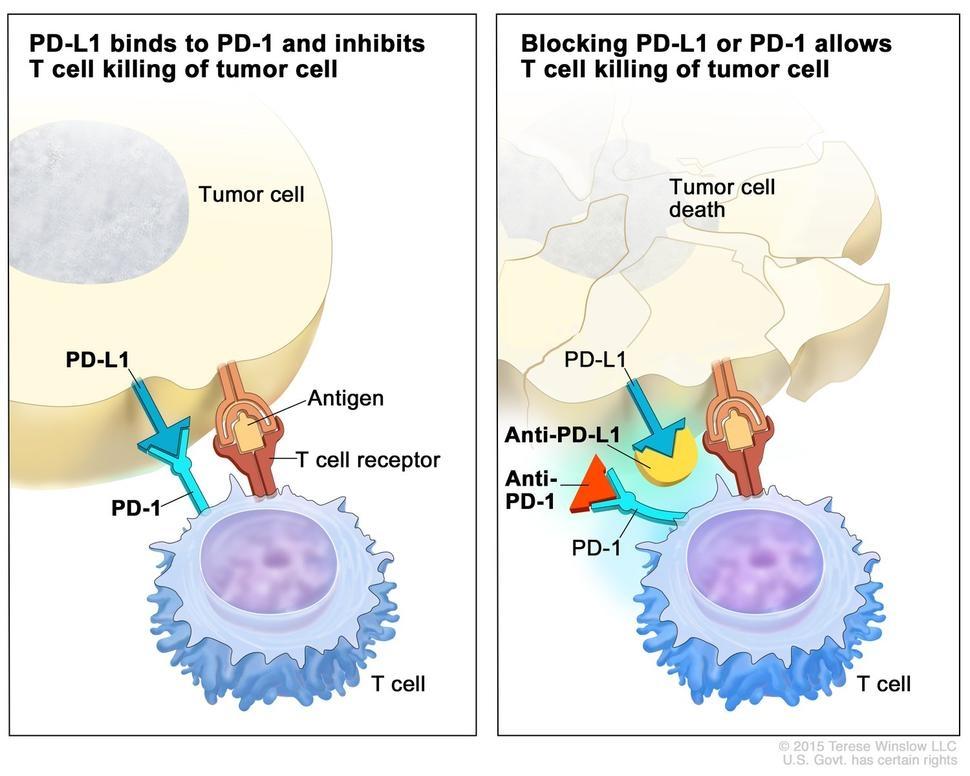
(Immune Checkpoint Inhibitors - NCI)
Drogcélpontok látása énn Valós interakciós hálózataik
XL-MS (keresztkötő tömegspektrometria) Egy nagyon egyszerű ötletből indul ki: ha két fehérje elég közel van egymáshoz, egy keresztkötő összezárhatja őket. Amint ez a kapcsolat létrejött, a tömegspektrometria képes kimutatni a keresztkötő peptideket, és megmutatja, mely régiók érintettek a fehérjéknek.
In practice, this means that you can add cross-linking agents directly to cell lysates or purified complexes. These reagents create covalent bonds between nearby amino acids, effectively "freezing” protein - protein interactions in place. Importantly, this includes weak, transient, or condition-dependent interactions that often disappear during purification or washing steps.
A Drug Target Discovery esetében ez a részletesség rendkívül értékes. A legtöbb gyógyszercélpont nagy multifehérje komplexekben vagy jelátviteli útvonalakban működik. Ha csak egyetlen fehérje szerkezetét ismered, csak egy részt látsz a történetből. XL-MS-szel a következőket teheted:
• Térképezd fel, mely fehérjék lépnek közvetlenül kölcsönhatásba a célpontoddal
• Azonosítani a közelítő kötőhelyeket vagy doméneket, amelyek az interakcióban részt vesznek
•Összehasonlítsuk az egészséges és betegségminták közötti interakciómintákat
• Nyomon kövessék, hogy a jelölt vegyületek miként zavarhatják vagy stabilizálhatják a konkrét kontaktusokat
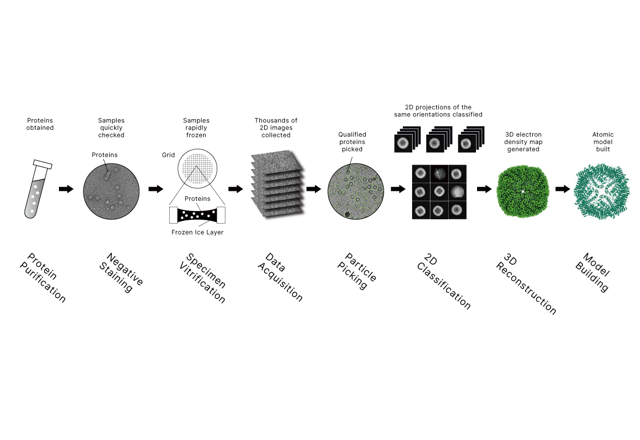
Az XL-MS jól kombinálható szerkezeti módszerekkel, mint például a krio-EM és a röntgenkristályográfia is. A szerkezetbiológia magas felbontású pillanatképeket ad. Az XL-MS távolságkorlátozásokat és interakciómintákat ad hozzá, amelyek segítenek a modellek validálásában vagy finomhangolásában, különösen nehezen megoldható rugalmas régiók esetében. Együtt élethűbb képet adnak arról, hogyan viselkedik a gyógyszercélpont egy zsúfolt molekuláris környezetben.
Miért illeszkedik az XL-MS a modern gyógyszercél-felfedezési folyamatokhoz
Sok csapat ugyanazt mondja: mélyebb betekintést akarnak a fehérje kölcsönhatásaiba, de nem engedhetik meg maguknak, hogy olyan módszert engedjenek meg, amely lassítja az egész programot. Az XL-MS vonzó, mert gazdag biológiai információkat nyújt anélkül, hogy teljes munkafolyamat-újratervezést igényelne.
Néhány gyakorlati előny kiemelkedik a mindennapi projektekben:
•Nagy áteresztőképesség, magas információtartalom
Az XL-MS jól alkalmas összetett mintákhoz és nagy vizsgálatokhoz. Miután a keresztkötés és az emésztés optimalizálásra került, a fejlett tömegspektrométerek egyetlen futás alatt sok mintát képesek kezelni. Az automatizált adatfeldolgozás ezután a nyers spektrumokat interakciós térképekké alakítja, segítve a csapatot gyorsabban haladni a kísérlettől az értelmezésig.
•Művei őshonosabb körülmények között
Mivel a keresztkötés sejtes vagy közel fiziológiai környezetben is elvégezhető, nem korlátozódik a magasan tisztított fehérjékre. Ez lehetővé teszi, hogy rögzítsd azokat a kölcsönhatásokat, amelyek csak bizonyos körülmények között alakulnak ki, például kofaktorok jelenléte, membránkörnyezet vagy betegséghez kapcsolódó stresszjelek. A Gyógyszer Cél Felfedezése esetén ez azt jelenti, hogy a jelölteket olyan kontextusban értékelik, amely jobban tükrözi az in vivo eseményeket.
• Nincs szükség speciális fehérjecímkézésre
Az XL-MS nem igényel egyedi kémiai címkéket vagy genetikai címkéket minden fehérjén. Ez csökkenti a kísérleti összetettséget, elkerüli a lehetséges artefakták jelölését, és megkönnyíti a skálázást sok célpont és feltétel felett.
•Érzékeny a gyenge és átmeneti interakciókra
A legfontosabb szabályozó események közé tartoznak az alacsony affinitású vagy rövid életű komplexumok. Pontosan ezek azok a kölcsönhatások, amelyek hagyományos lehúzásos vagy tisztításon alapuló technikákkal eltűnhetnek. A keresztlinkezés a bekövetkezésük pillanatában rögzíti őket, így teljesebb interakciós hálózatot ad, és segít elkerülni a vakfoltokat a Drug Target Discovery során.
Taken together, these benefits allow research teams to prioritize targets more intelligently. Instead of focusing only on what is easy to measure, you can focus on what is biologically meaningful - while still keeping timelines and budgets under control.
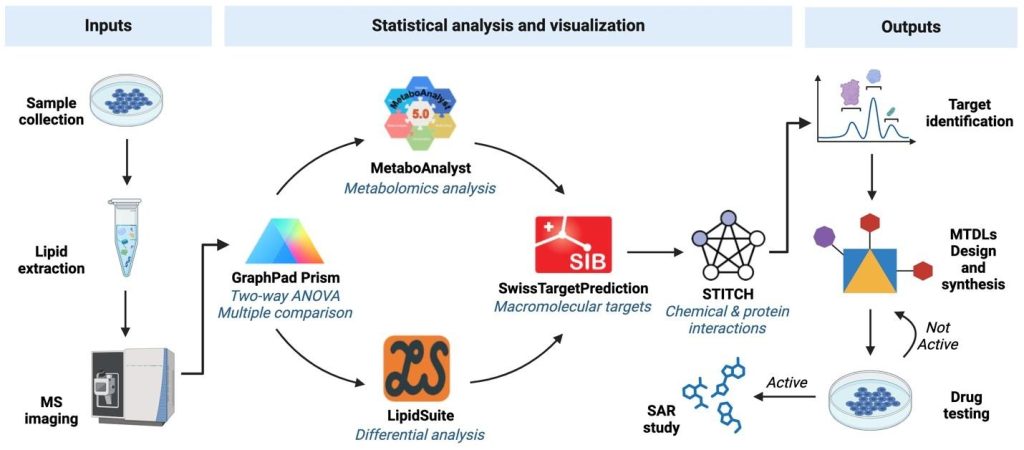
(Többcélzott irányú ligandok és lipidómiai megközelítés glioblastoma gyógyszer felfedezéséhez)
Hogyan támogatja a Longlight technológia az XL-MS munkafolyamatokat végponttól végpontig
A Longlight Technology-nál az XL-MS-et nem egyetlen kísérletként, hanem egy integrált megoldásként pozícionáljuk a gyógyszercél felfedezésére. Sok csoportnak nincs meg a belső sávszélessége ahhoz, hogy teljes XL-MS vezetéket építsen a nulláról, ezért szolgáltatásainkat úgy tervezzük, hogy illeszkedjenek a meglévő kutatási folyamatodhoz.
You can either send us pre - cross-linked samples, or collaborate with our scientists to define a cross-linking strategy tailored to your system - choosing appropriate cross-linkers, conditions, and controls. From there, Longlight Technology takes care of every technical step, including sample digestion, cross-linked peptide enrichment, mass spectrometry acquisition, and data analysis. You receive a clear, project-ready report that maps protein interaction partners, identifies cross-link sites, and distills the structural information most relevant to your target and mechanism-of-action decisions.
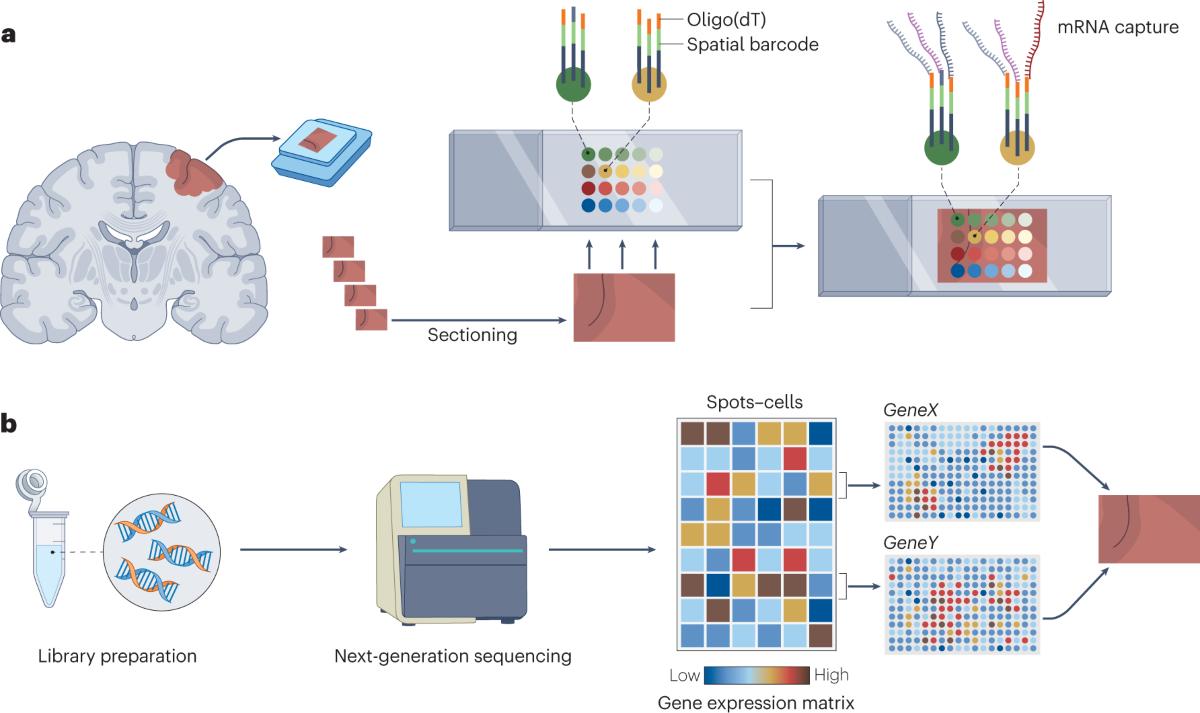
Beyond XL-MS, Longlight Technology also supports the upstream and downstream work that surrounds Drug Target Discovery. Our genomics solutions, including next-generation sequencing - related instruments and reagents, help you identify genetic variants, expression changes, and regulatory elements linked to disease pathways. Techniques such as ChIP-seq connect protein - DNA interactions to the protein - protein interaction maps generated by XL-MS, giving you a broader view of how targets sit within chromatin regulation and transcription networks.
To keep your lab running smoothly, we also provide a range of consumables and kits - such as nucleic acid extraction kits, library preparation kits, precast agarose gels, and specialized tubes - that are designed for consistent, everyday use in research and biopharmaceutical environments. The mission is to simplify every stage - preparation, measurement, and analysis - so your scientists can spend less time on setup and troubleshooting, and more time testing hypotheses that matter. Bringing together XL-MS for interaction mapping, genomics platforms, and stable lab tools delivers a more coordinated and effective Drug Target Discovery workflow. Instead of isolated experiments, you build a pipeline that continually feeds better data into better decisions.
Ha a szervezete a felfedezési ciklusok rövidítését, a kockázat csökkentését és tisztább képet akar szerezni arról, hogyan viselkednek a potenciális gyógyszercélpontok a valódi biológiai rendszerekben, örömmel támogatnánk Önt.
Érdekel, hogy felfedezze az XL-MS-et a következő Gyógyszercél Felfedező projektedhez?
Vegye fel a kapcsolatot a Longlight Technology-vel, hogy megbeszélje célpontjait, mintáit vagy tanulmánytervét, és segítsünk abban, hogy a bonyolult fehérjekölcsönhatási adatokat konkrét, gyakorlati betekintéssé alakítsák.