Kapcsolódó bejegyzés
A nagy teljesítményű ultrahangos készülék laboratóriumhoz megakadályozza a reprodukálhatósági hibákat
2025-09-24
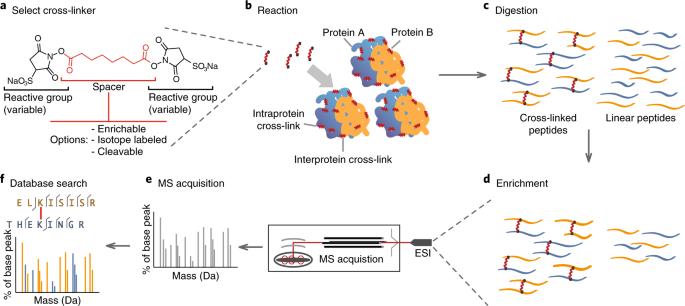
Elemzés membránfehérjékről XL-MS-szel: lépésről lépésre munkafolyamat útmutató
2026-02-20

Nagy pontosságú genomikai laboratóriumi képalkotó rendszer ultratiszta optikai technológiával
2025-07-31
Elemzés membránfehérjékről XL-MS-szel: lépésről lépésre munkafolyamat útmutató
2026-02-20Az XL-MS-szel végzett membránfehérjék elemzése az egyik leggyakorlatiabb módja annak, hogy a "nehezen látható" membránkölcsönhatásokat mérhető bizonyítékká alakítsuk. A Longlight Technology kémiai keresztkötést és tömegspektrometriát (XL-MS) használ, hogy segítse a kutatókat fehérje–fehérje kölcsönhatások (PPI-k) feltérképezésében, gyenge vagy rövid életű kontaktok rögzítésében, valamint a hipotézisektől védhető szerkezeti modellekre való áttérésben – anélkül, hogy speciális kémiai címkézési munkafolyamatokat kényszerítene rá.
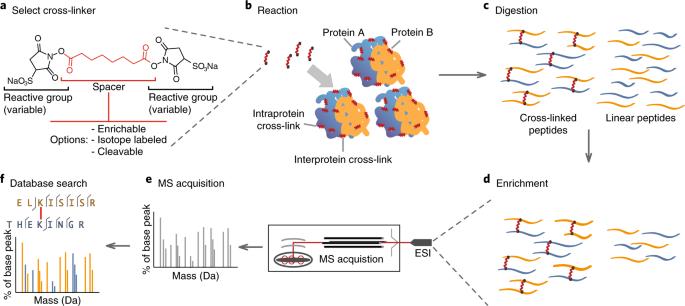
Keresztkötésű tömegspektrometria: módszerek és alkalmazások szerkezeti, molekuláris és rendszerekben
Mi az az XL-MS? Mik azok a membránfehérjék?
Az XL-MS és a membránfehérjék két olyan elképzelés van, amely gyakran együtt jelenik meg a szerkezeti biológiában és a gyógyszerkutatásban. Itt egy világos, kezdőbarát magyarázat.
Mi az az XL-MS?
XL-MS A keresztkötő tömegspektrometria (gyakran kémiai keresztkötő és tömegspektrometria kombinációjaként írják).
Ez egy olyan módszer, amelyet a fehérje–fehérje kölcsönhatások és fehérje alakok tanulmányozására használnak két dolog segítségével:
Keresztkötés (XL): "Fagyasztás" a közeli részeket a helyükön
Egy kémiai keresztkötés úgy működik, mint egy apró molekuláris "híd". Ha két aminosav-hely elég közel van egymáshoz a valós térben (rövid távolságon belül), a keresztkötő kovalens módon összekapcsolhatja őket.
Ez segít megőrizni azokat a gyenge vagy rövid életű kölcsönhatásokat, amelyek a normál mintakezelés során széteshetnek.
Tömegspektrometria (MS): Azonosítsd a kapcsolódó darabokat
A keresztkötés után a fehérjéket peptidekké emésztőznek. A tömegspektrométer keresztláncolt peptidpárokat érzékel, és szoftver visszatérképezi őket fehérjékre.
Ezek a kapcsolatok távolsági nyomokat (térbeli korlátozásokat) adnak, amelyek megmondják, mely régiók voltak közel az eredeti komplexumban.
Amit az XL-MS (gyakorlatban):
• Melyik fehérjék valószínűleg kölcsönhatásba lépnek (interakciós hálózat)
• Mely régiók érintik egymást (interfész tippek)
• Strukturális korlátok, amelyek támogatják a modelleket (gyakran krio-EM vagy röntgen kombinációval)
Mik azok a membránfehérjék?
A membránfehérjék olyan fehérjék, amelyek egy sejtmembránba (vagy sejteken belüli membránokhoz, mint például az ER, a mitokondriumok vagy baktériumok membránjaihoz) vannak beágyazódva vagy ahhoz rögzítve.
Kritikusak, mert a membránok irányítják a szállítást és a jelátvitelt, míg a membránfehérjék gyakran "kapuőrökként" vagy "antennáként" működnek a sejt számára.
Fő típusok
• Integrált membránfehérjék: fizikailag beágyazva a membránba
• Sok egy-két alkalommal átfedi a membránt (gyakran transzmembrán fehérjéknek nevezik)
• Perifériás membránfehérjék: a membrán felszínéhez kötve (gyakran más fehérjék vagy lipidek révén)
Miért számítanak a membránfehérjék
• Részt vesznek a következőkben:
• Szállítás (csatornák, szivattyúk, szállítók)
• Sejtjelátvitel (receptorok, mint a GPCR-ek)
• Energiaátalakítás (légzéslánc komplexumok)
• Sejtfelismerés és tapadás
Miért "nehezek"
A membránfehérjék vizsgálata kihívást jelent, mert:
• Lipid környezetben ülnek
• A membránból eltávolítva instabilak lehetnek
• Gyakran dinamikus komplexumokat alkotnak, amelyek állapotokat változtatnak
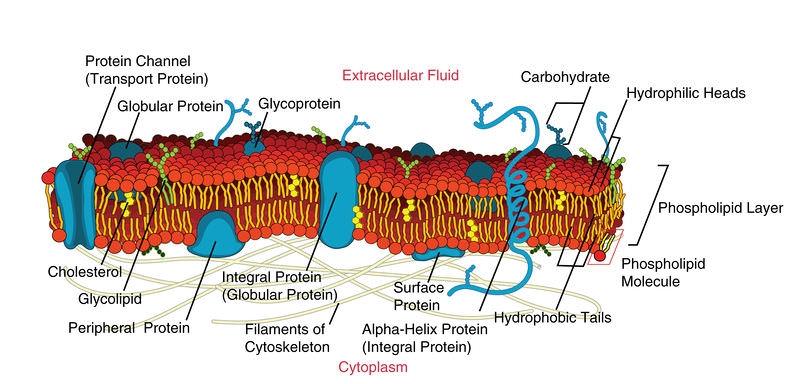
Membrane Proteins - Biology LibreTexts
Miért van szükség membránfehérjéknek egy Más stratégia
A membránfehérjék gyakran zsúfolt, dinamikus környezetben helyezkednek el. Kulcsfontosságú interfészeik átmeneti lehetnek, és sok komplex instabil, miután eltávolítják a membránból. Ezért a klasszikus interakciós módszerek elkerülhetik a kritikus kontaktusokat, vagy túlzottan egyszerűsíthetik a folyamatot.
Az XL-MS-szel működő membránfehérjék elemzése azért működik, mert keresztkötési szerekkel "lefagyasztja" a közeli területeket. Ezek a reagensek kovalentálisan összekapcsolhatnak két vagy több kölcsönhatásban lévő fehérjét egy meghatározott távolsági ablakon belül. Miután a kölcsönhatás rögzített, a tömegspektrometria képes kiolvasni a keresztkötő peptideket, és a valószínű kontaktpontokra irányítani. Működési szempontból az interakciós bizonyítékok nyomon követhetők még akkor is, ha a komplexek gyengék.
• Biztosítja a rövid életű kölcsönhatásokat, amelyek gyakran elvesznek a tisztítás során
• Kerüli a vegyi címkézést, egyszerűsítve a korai döntéseket
• Lehetővé teszi a sejten belüli keresztkötést, hogy megőrizze a natív közelséget
1. lépés: Határozd meg a biológiai kérdést és a távolsági indoklást
Döntsd el, mit szeretnél tanulni, mielőtt elkezdenéd. Megerősíted a gyanús partnert? Mutáns és vad típusú kötés összehasonlítása? Egy interfész modell támogatására térképezni? Egy világos kérdés segít kiválasztani a feltételeket, az irányítást és az adatkimeneteket.
Az XL-MS távolsági információval rendelkezik. A keresztkötési ügynökök olyan maradékokat kötnek össze, amelyek közel vannak a térben, nem feltétlenül egymáshoz közel. A membránfehérjék esetében ez a távolságlogika értékes, mert feltárhatja, hogyan csomagolódnak a hélikék, hogyan találkoznak a citozolikus hurkok, vagy hogyan állnak össze az oligomerek.
Egy kezdőbarát módja a terv megfogalmazásának, ha három kimenetet határozz meg:
• Interakciós jelenlét: egyáltalán kapcsolatba lép A B-vel?
• Interakció topológia: A mely régiói érintkeznek B melyik régiójával?
• Helyszíni bizonyíték: mely peptidpárok támogatják az interakciós hálózatot?
Az XL-MS-szel történő membránfehérjék elemzése sokkal gördülékenyebbé válik, ha előre eldöntöd, melyikre van szükséged a következő döntésedhez (szerkezeti modellezés, célpont validálás vagy mechanizmustanulmány).
2. lépés: Válassz egy Keresztkötő megközelítés, amely illeszkedik a membrán kontextushoz
A membránfehérjék érzékenyek a mosószerekre, a lipid mimetikusokra és a pufferösszetételre. A cél az, hogy a lehető legközelebb hasonlítson a funkcionális komplexumhoz hasonló állapotot fenntartani, majd a megfelelő pillanatban keresztlinkelni.
A Longlight Technology-nál az ügyfelek vagy már kereszt-összekapcsolt mintákat küldhetnek, vagy felvehetik velünk a kapcsolatot, hogy keresztkapcsolati tervet dolgozzanak ki, majd mintákat küldjenek. Ez a rugalmasság fontos membráncélok esetében, mert az egyik projekt megoldáson belüli keresztkötést igényelhet, míg a másik a bennszülöttebb körülmények vagy akár sejten belüli keresztkötés is előnyös.
✔ A nagy áteresztőképesség és a gyors elemzési sebesség lerövidítheti az iterációs ciklusokat
✔ Az intracelluláris keresztkötés csökkentheti a túlzott kezelési komplexumok okozta artefaktumokat
✔ Nincs külön címkézési követelmény, így a korai kísérletek hozzáférhetővé válnak
Gyakorlati tipp kezdőknek: tervezz legalább egy negatív kontrollt (nincs keresztkötő vagy partnerfehérje), és ha van egy "ismert viselkedés" referencia. A vezérlők segítenek megkülönböztetni a valós közelségi jeleket a háttértől.
3. lépés: Keresztkötésű fehérjékből to Észlelhető peptidek
A keresztkötés után a munkafolyamatnak le kell fordítania a fehérjéket peptidkeverékté, amely még mindig megőrzi a keresztkötési információkat. Itt sok kezdő elveszettnek érzi magát, mert a keresztkötő peptidek ritkábbak, mint a normál peptidek, és nehezebben észlelhetők.
Szabványos szolgáltatási munkafolyamatunk a teljes láncot lefedi:
• Enzimemésztés
• Peptid dúsítás
• Tömegspektrometriai detektálás
• Adatelemzés
• Kísérleti jelentés kiadása
A kulcsötlet egyszerű: az emésztés peptidté alakítja a fehérjéket, a dúsítás növeli a keresztkötő fajok relatív láthatóságát, a tömegspektrometria pedig a peptid tömegeket és fragmentumokat méri, hogy a szoftver keresztkötőpárokat is meg tudjon rendelni.
Az XL-MS-szel történő membránfehérjék elemzése a leghatékonyabb, ha a mintakészítést információmegőrzési lépésként kezeljük, nem csupán rutinprotokollként. A legjobb eredmények stabil emésztés és gondos gazdagítás révén születik, így az adatok elegendő jelet hordoznak a magabiztos értelmezéshez.
4. lépés: Tömegspektrometria kiolvasó egynd Interakciós Hálózat Leképezés
A tömegspektrometria többet tesz annál, mint "fehérjék azonosítása". Az XL-MS-ben keresztkötő peptidpárokat azonosít, amelyeket térbeli korlátozásként értelmezhetünk. Ha elég nagy megbízhatóságú linked van, elkezdheted ábrázolni az interakciós hálózatokat és következtetni az akcióhelyeket – különösen hasznos összetett membrán-összeállítások esetén.
Itt válik az XL-MS hidat a szerkezeti biológiához. Sok csapat XL-MS kimeneteket használ a cryo-EM vagy röntgenkristályográfia mellett. A kereszthivatkozási bizonyítékok segíthetnek:
• Validálja, hogy egy szerkezeti modell hiteles-e
• Feloldani a kétértelmű alegységek orientációit
• Támogatja a domain elhelyezést, ha a sűrűség korlátozott
Más szóval, az XL-MS-szel történő membránfehérjék elemzése átmozdíthat a "úgy gondoljuk, hogy ez a két régió kölcsönhatásba lép" állapotból ahhoz, hogy "távolsági bizonyítékunk van, ami korlátozza a modellt".
5. lépés: Hogyan to Olvasd tJelentés egyés az adatokat következő kísérletekké alakítani
Egy jelentés csak akkor értékes, ha irányítja a döntéseket. Kezdőknek a leghasznosabb módja az XL-MS eredmények olvasásának, ha mintákat keresünk, nem csak listákat.
Kezdjük három kérdéssel:
✔ A keresztkapcsolatok reprodukálhatók-e replikátumok vagy körülmények között? A reprodukálhatóság önbizalmat épít.
✔ A linkek konkrét régiókban csoportosulnak? A klaszterezés gyakran valódi interfészekre utal.
✔ Megváltoztatják a mutáns/ligand állapotok a kapcsolati mintát? A váltások felfedhetik a mechanizmust.
Ezután a bizonyítékokat a következő lépésekké fordítsd át. Ha a linkek támogatnak egy adott interfészt, akkor pontmutációkat tervezhetsz validációhoz. Ha a linkek váratlan partnereket ajánlanak, akkor ortogonális megerősítést tervezhetsz. Ha a kapcsolatok korlátozzák a modellt, nagyobb magabiztossággal folytathatod a szerkezeti finomítást.
CTA: Ha XL-MS-szel szeretnél membránfehérjéket elemezni, de nem vagy biztos abban, hogyan válassz feltételeket vagy kontrollokat, vedd fel a kapcsolatot a Longlight Technology-vel, hogy keresztkapcsolati tervet dolgozzon ki, és teljes munkafolyamat-jelentést kapj – az emésztéstől az adatelemzésig. Kérjen ingyenes árajánlatot, hogy elindítsd projektedet egy világos, kezdőbarát kísérleti úttervvel.
Miért a Longlight technológia? fvagy XL-MS egynd Beyond
A membránfehérje projektek ritkán élnek egyetlen technikában. Általában platformszemléletet igényelnek: megbízható mintakezelést, szigorú adatokat és az iterációt felgyorsító eszközöket.
A Longlight Technology átfogó támogatást nyújt csúcstechnológiás genomikai megoldásokkal, fejlett laboratóriumi eszközökkel, valamint magas minőségű reagensekkel és fogyókeszközökkel, amelyek a modern laboratóriumok hatékonyságának és pontosságának javítására szolgálnak. Az XL-MS szolgáltatások mellett támogatjuk a kutatócsoportokat genomikai és molekuláris biológiai eszközökkel, beleértve az NGS-hez kapcsolódó eszközöket, például fókuszált ultrahangrendszereket, valamint széles körben használt fogyókeszközöket és készleteket (előre gyártott agarózzélek, nukleinsav-kivonási készletek és könyvtárkészítő készletek) akadémiai, klinikai és ipari alkalmazásokhoz.
Az XL-MS-szel történő membránfehérjék elemzése nemcsak módszer – hanem egy munkafolyamat-tudományág. Amikor a munkafolyamat stabil, a következtetéseid világosabbak lesznek, a modellek védhetőbbek, és a következő kísérleted könnyebben megtervezhetővé válik.